关节处软骨细胞由于缺乏血供和神经支配,自我修复能力有限。这使得临床上关节软骨的再生是一个巨大挑战。细胞疗法被认为是修复受损关节软骨的重要方法。骨髓间充质干细胞由于其多向分化潜能和免疫调节能力,已成为关节软骨修复的潜在治疗手段。临床实验证明这类间充质干细胞对软骨类疾病具有一定的改善。但是这些干细胞往往形成纤维软骨或者在修复过程中展示出副作用,且在体外扩培的过程中容易衰老,其分化潜能会因为患者衰老而减弱。其他来源的间充质干细胞仍然需要大量临床研究证实其修复潜能。因此,研究越来越热衷于探索和测试其他与软骨再生有关的种子细胞。
侧板中胚层是关节软骨的发育起源之一,经历间充质、间充质凝聚体发育成软骨。这个发育过程中存在多种可发育为软骨的前体细胞。因此四川大学李中瀚教授团队提出一种新的软骨再生策略,即研究与四肢骨发育相关的分化路径和互作的关键信号,再基于诱导性多能干细胞模拟软骨发育过程进行阶段式的体外分化,得到具有软骨修复潜力的种子细胞,用于关节软骨的再生修复。

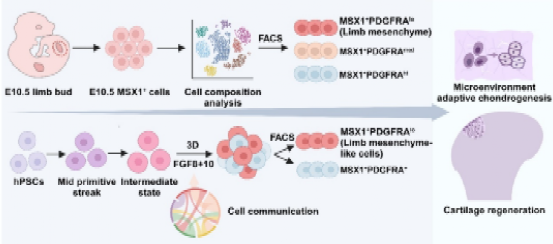
2024年2月29日,四川大学李中瀚教授研究团队在Stem Cell Reports上发表题为“MSX1+PDGFRAlow limb mesenchyme-like cells as an efficient stem cell source for human cartilage regeneration”的研究论文。该研究为获取可用于软骨组织修复的种子细胞,首先基于MSX1P2A-tdTomato基因敲入小鼠,研究了胚胎时期后肢MSX1+细胞的分化潜能及软骨再生效果。通过单细胞转录组测序,分析了小鼠早期肢芽细胞的异质性,并结合体内分化和软骨修复实验证明了MSX1+PDGFRAlow肢芽间充质是决定发育和再生潜能的细胞亚群。对人5周胎儿的肢芽单细胞数据进行分析,同样解析到了PDGFRA标记的侧板中胚层细胞以及MSX1+PDGFRAlow的肢芽间充质细胞。最后是利用CRISPR/Cas9构建了MSX1P2A-tdTomato基因敲入的hPSCs细胞系,通过模拟发育过程,进行体外分化得到了具有极性的侧板中胚层和肢芽间充质类细胞群。并且证明了MSX1+PDGFRAlow的肢芽间充质类细胞同小鼠原代细胞一样,也决定了发育潜能和软骨修复能力。
在本研究中,四川大学博士生廖远松作为该论文第一作者,四川大学李中瀚教授、祝卿副主任医师作为该论文的共同通讯作者。该研究获得了科技部重点研发计划“干细胞研究与器官修复”和“干细胞及转化研究”项目、国家自然科学基金、国家特聘计划青年项目、四川大学理科原创基金等的资助。
原文链接:
https://doi.org/10.1016/j.stemcr.2024.02.001
